【酸と塩基の見分け方や定義】って
「なんとなく分かるけどちゃんと説明できない」
という人は多いのではないでしょうか?
今回はそんな酸と塩基について分かりやすく
詳しく解説します。
酸と塩基の定義
酸と塩基についてとっても簡単にいうと
・酸→酸っぱい
・塩基→苦い,ヌルヌル
ただもちろん中学や高校のテストで
味で答えるのは許されないので
化学的に酸と塩基の違いを説明できる
アレニウスの定義と
ブレンステッドローリーの定義を
解説します。
アレニウスの定義 (酸)
・酸→水中でH+を生じる物質
(例:塩酸)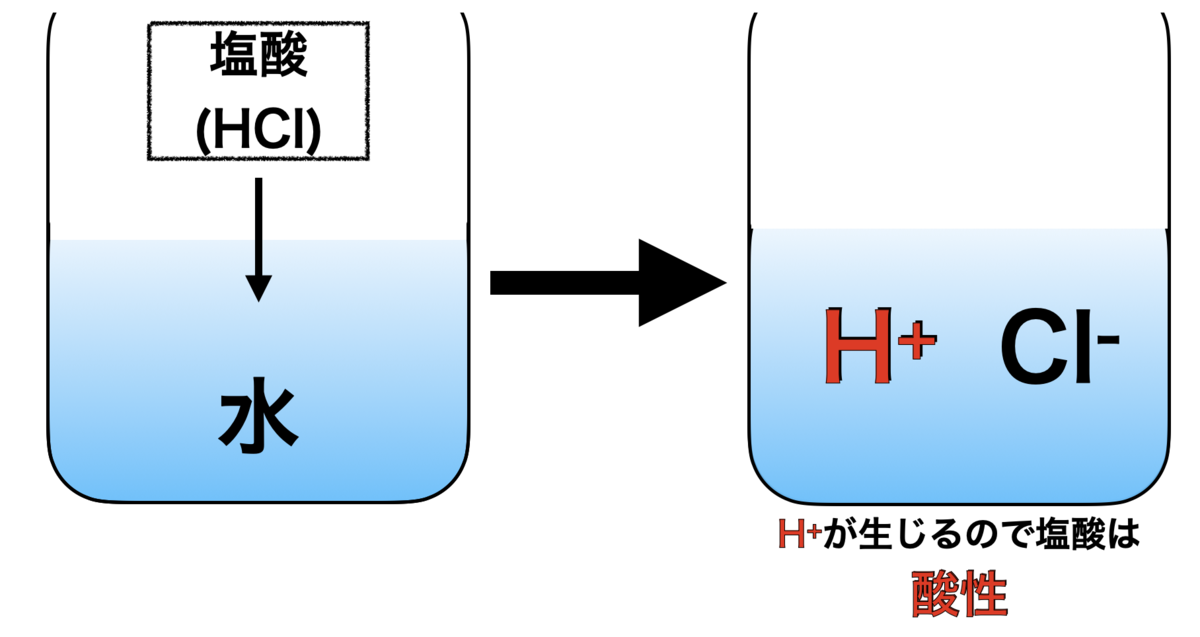 [反応式 : HCl→H++Cl-]
[反応式 : HCl→H++Cl-]
アレニウスの定義 (塩基)
・塩基→水中でOH-を生じる物質
(例:水酸化ナトリウム)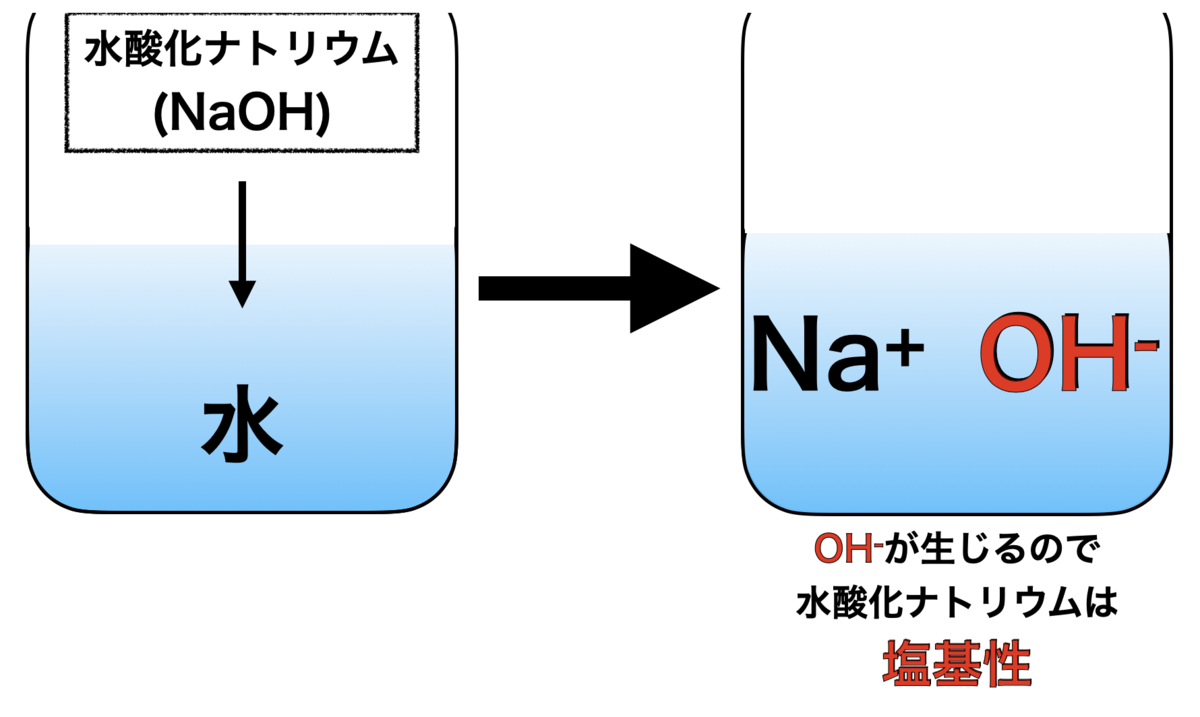 [反応式 : NaOH→Na++OH-]
[反応式 : NaOH→Na++OH-]
アレニウスの定義のメリット
アレニウスの定義のメリットは
とても分かりやすいことです。

先ほど紹介した水中で分解(電離)した物質の
化学式を見ればH+やOH-があるので
酸か塩基の判断が容易にできます。
アレニウスの定義のデメリット
逆にアレニウスの定義のデメリットは
一部の物質相手にしか使えないと
水中でしか判別できないの2つあります。
例えば
アンモニア(NH3)は塩基性ですが
NaOHと違ってOH-を持っていないので
アレニウスの定義では判別ができません。
NH3 ←塩基なのにOH-がない
このように一部の物質には使えないのが
アレニウスの定義のデメリットです。
ブレンステッドローリーの定義 (酸)
・酸→H+を相手に与える物質
(例:塩酸) [反応式 : HCl→H++Cl-]
[反応式 : HCl→H++Cl-]
上図を詳しく表すと下図になる。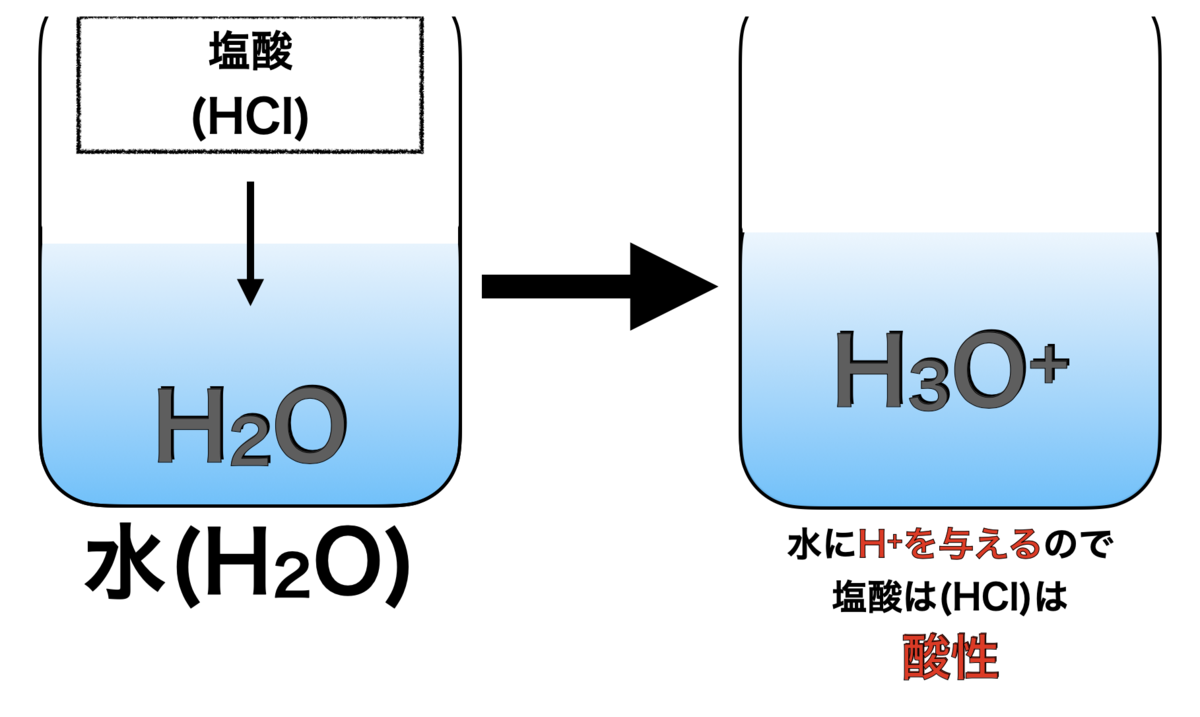 [反応式:HCl+H2O→ H3O++Cl-]
[反応式:HCl+H2O→ H3O++Cl-]
このように塩酸が水にH+を与えているので
塩酸は酸性といえる。
※H3O+とはオキソニウムイオンのこと
(よく省略してH+と表される)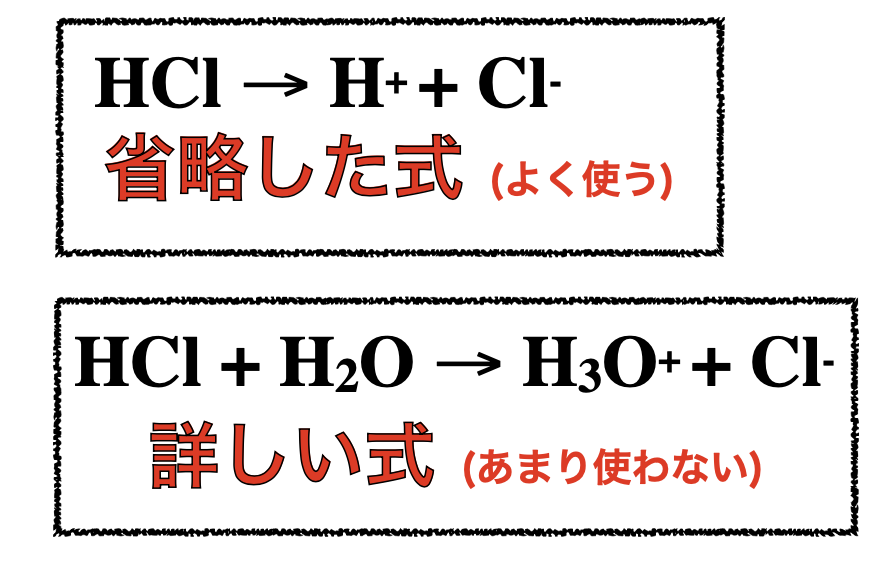 この2つの式は基本的に同じ意味ですが
この2つの式は基本的に同じ意味ですが
省略した上の式がよく使われます。
※オキソニウムイオン(H3O+)は
頭の片隅に入れとくと便利です。
ブレンステッドローリーの定義(塩基)
・塩基→H+を受け取る物質
(例:アンモニア)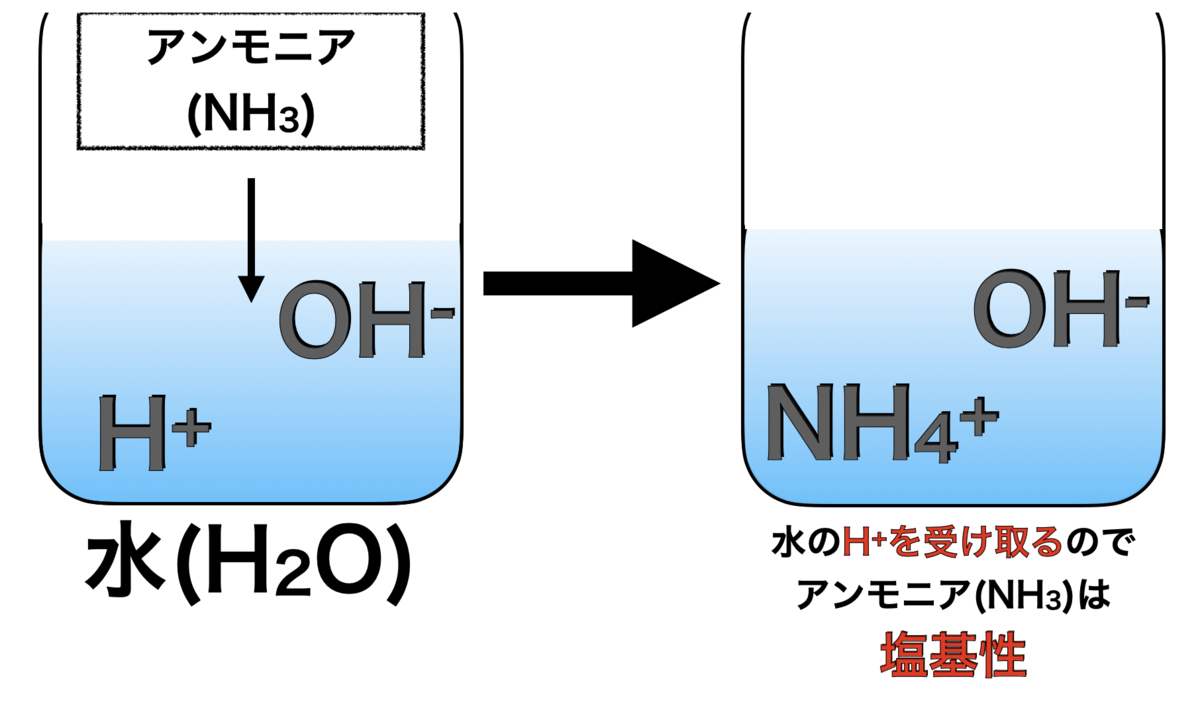 [反応式:NH3+H2O→ NH4++OH-]
[反応式:NH3+H2O→ NH4++OH-]
アンモニア(NH3)が水からH+を受けとるので
アンモニアは塩基と言える。
ブレンステッドローリー
の定義のメリット
ブレンステッドローリー定義のメリットは
万能でさまざまな物質に使えることです。
例えばアレニウスの定義では判別できない
アンモニア(NH3)も判別できます。
ブレンステッドローリー
の定義のデメリット
ブレンステッドローリー定義のデメリットは
とにかく分かりにくいことです。
オキソニウムイオンが出てくるし
塩基でもOH-じゃなくてH+の動きで判別するので
イメージでしにくいです。
まとめ
アレニウスの定義
・酸→水中でH+を生じる物質 [反応式 : HCl→H++Cl-]
[反応式 : HCl→H++Cl-]
・塩基→水中でOH-を生じる物質 [反応式 : NaOH→Na++OH-]
[反応式 : NaOH→Na++OH-]
アレニウスの定義の特徴
アレニウスの定義は分かりやすいけど
水中でしか使えないし一部の物質には使えない。
例えば
アンモニア(NH3)は塩基性だが
NaOHと違ってOH-を持っていないので
アレニウスの定義では判別ができない。
ブレンステッドローリーの定義
・酸→H+を相手に与える物質 (省略した式)
(省略した式)
[反応式 : HCl→H++Cl-]
(詳しい式)
[反応式:HCl+H2O→ H3O++Cl-]
・塩基→H+を受け取る物質 [反応式:NH3+H2O→ NH4++OH-]
[反応式:NH3+H2O→ NH4++OH-]
ブレンステッドローリー
の定義の特徴
OH-じゃなくてH+の動きで判別するので
分かりにくいが万能で様々な物質に使える。
例:アンモニア(NH3)
今回は以上です。
ご覧いただきありがとうございました。
もし「良いね」って思っていただけたら
下から読者登録していただけると嬉しいです。