あなたは単体,化合物,混合物の違いが
分かるような分からないような...って
放置したままにしてませんか?

今回は単体,化合物,混合物の違いを
解説していきます。
単体と化合物と混合物の違い
まず、単体,化合物,混合物の違いを調べると
純物質も加わって次のように4種類出てきます。


物質は混合物と純物質に分けられ
次にその純物質が単体と化合物に分けられます。
続いてこの種類を
超簡単に見分ける手順を紹介します。
見分ける手順

手順1: 物質名を化学式にする
手順1で、物質を混合物or純物質に分けます。
手順2:化学式の大文字を数える
手順1で純物質だった場合、
手順2で単体or化合物に分けます。
このように、2ステップだけで
単体,化合物,混合物を分けることができるのです。
実際に例を使って見分けていきましょう。
見分ける手順の例
手順1
まずは手順1「物質名を化学式にする」で
混合物or純物質を判別します。
例:塩化ナトリウム水溶液(NaCl,H2O)
NaClとH2Oの2つの化学式で表せるので
塩化ナトリウム水溶液は混合物といえます。
手順2
次は手順2「化学式の大文字の数を数える」で
以下の3種類の純物質を単体or化合物に
分けてみましょう。
例:①塩化ナトリウム(NaCl)
②ナトリウム(Na)
③塩素(Cl2)
さっそく化学式の大文字を数えると
① NaCl→2つ
② Na→1つ
③ Cl2→1つ なので
答え
①塩化ナトリウム(NaCl)→化合物
②ナトリウム(Na)→単体
③塩素(Cl2)→単体
単体は1つの元素で化合物は2つ以上の元素からできているので
大文字1つ→単体
大文字2つ以上→化合物であるといえます。
⚠️塩素(Cl2)は2がついてるので化合物と間違えやすいですが
2は分子の数を表すだけで今回重要なのは元素の種類。
「元素の種類」=「化学式の大文字の数」なので
大文字1つで書ける塩素(Cl2)は単体です。www.kemisupea.com
まとめと実践的な例題
単体,化合物,純物質,混合物の違い
・単体→1種類の元素からなる物質
・化合物→2種類以上の元素からなる物質
・純物質→1種類の成分でできた物質
・混合物→2種類以上の純物質が混ざった物質
手順1. 物質名を化学式にする
→複数の化学式になるなら混合物,
→1つの化学式なら純物質(単体or化合物)なので
手順2で判別
手順2. アルファベットの大文字の数を数える
→大文字が1つなら単体,
→大文字が2つ以上なら化合物
手順1→純物質or混合物を判別
手順2→単体or化合物を判別
まとめ例題1
次の物質を単体or化合物に
分類してください
手順1:まずは全部化学式にします。↓
手順2:左から順に大文字を数えると
2つ,1つ, 1つ, 3つ, 1つなので
下の表のように簡単に分けられます。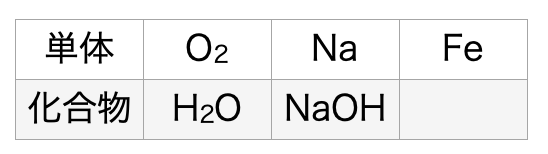
まとめ例題2
次の物質を単体,化合物,混合物に分類してください
・水
・ナトリウム
・水酸化ナトリウム
・空気
・水酸化ナトリウム水溶液
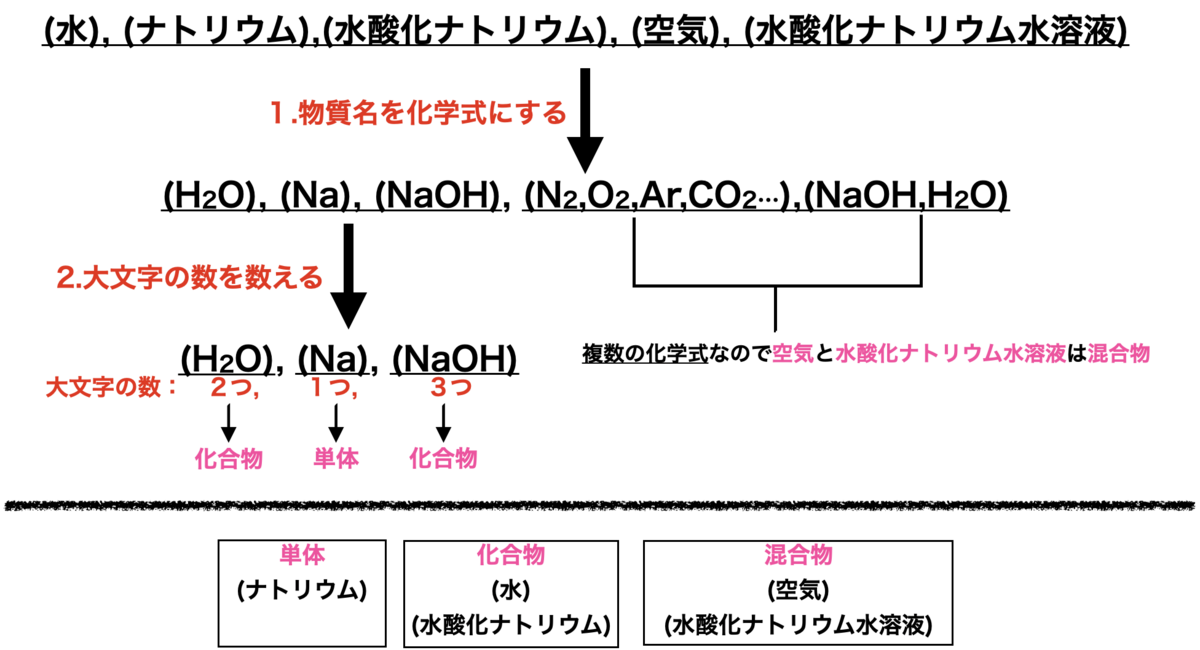
今回は以上になります。
元素,原子,分子の違いについても解説してるので
よかったら見てください。